作者:杉杉
导读:
近日,Oxford大学的S. P. Fletcher课题组在J. Am. Chem. Soc.中发表论文,报道一种全新的通过铑催化剂促进的二氢吡啶衍生物与芳基硼酸之间的不对称交叉偶联反应方法学,进而成功完成一系列手性3-哌啶分子的构建。
Catalytic Enantioselective Synthesis of 3‑Piperidines from Arylboronic Acids and Pyridine
S.Mishra, S.Karabiyikoglu, S. Fletcher, J. Am. Chem. Soc. 2023, ASAP. doi: 10.1021/jacs.3c05044.

正文:
手性哌啶骨架广泛存在于各类天然产物以及药物分子中 (Figure 1)。并且,在过去的几十年里,已经成功设计出多种构建手性哌啶分子的合成转化策略 (Scheme 1A)[1]-[2]。这里,受到近年来对于选择铑催化剂促进的通过张力烯基化合物以及双环烯基化合物参与的金属碳化过程 (carbometallation)[3]-[4]相关研究报道的启发,Oxford大学的S. P. Fletcher课题组成功设计出一种全新的通过铑催化剂促进的二氢吡啶衍生物与芳基硼酸之间的不对称交叉偶联反应方法学 (Scheme 1B)。


首先,作者进行二氢吡啶底物的合成研究 (Scheme 2)。

之后,作者采用phenyl carbamate dihydropyridine 1a与苯硼酸2a作为模型底物,进行相关反应条件的优化筛选 (Table 1)。进而确定最佳的反应条件为:采用[Rh(cod)(OH)]2作为催化剂,(S)-Segphos作为手性配体,Aq. CsOH作为碱, THP:甲苯:H2O (1:1:1 v/v/v)作为反应溶剂,反应温度为70 oC,最终获得81%收率的交叉偶联产物3a (96% ee)。

在上述的最佳反应条件下,作者分别对一系列芳基硼酸底物 (Scheme 3)与二氢吡啶以及二氢喹啉底物 (Scheme 4)的应用范围进行深入研究。




之后,该小组通过如下的一系列研究进一步表明,这一全新的对映选择性交叉偶联策略具有潜在的合成应用价值 (Scheme 5)。

接下来,作者对上述不对称交叉偶联过程的反应机理进行进一步研究 (Scheme 6A)。并基于上述的实验研究,提出如下合理的反应机理 (Scheme 6B)。


总结:Oxford大学的S. P. Fletcher课题组成功设计出一种全新的通过铑催化剂促进的二氢吡啶衍生物与芳基硼酸之间的不对称交叉偶联反应方法学,进而成功完成一系列手性3-哌啶分子的构建。这一全新的对映选择性交叉偶联策略具有广泛的底物应用范围、优良的官能团兼容性以及优良的区域与对映选择性等优势。
参考文献:
- [1] G. J. Brizgys,; H. H. Jung, P. E. Floreancig, Chem. Sci. 2012, 3, 438. doi:10.1039/C1SC00670C.
- [2] N. Kratena, B. Marinic, T. J. Donohoe, Chem. Sci. 2022, 13, 14213. doi:10.1039/D2SC04638E.
- [3] C. M. So, S. Kume, T. Hayashi, J. Am. Chem. Soc. 2013, 135, 10990. doi:10.1021/ja406169s.
- [4] L. Dian, I. Marek, Angew. Chem. Int. Ed. 2018, 57, 3682. doi:10.1002/anie.201713324.
- [5] (a) J. Bexrud, M. Lautens, Org. Lett. 2010, 12, 3160. doi: 10.1021/ol101067d.
- (b) F. Menard, M. Lautens, Angew. Chem. Int. Ed. 2008, 47, 2085. doi: 10.1002/anie.200704708.
- [6] F. W. Goetzke, A. M. L. Hell, L. van Dijk, S. P. Fletcher, Nat. Chem. 2021, 13, 880. doi: 10.1038/s41557-021-00725-y.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载
本文作者:杉杉
导读
近日,中国科学技术大学的王川课题组在ACS Catal.中发表论文,报道一种全新的通过镍催化剂促进的芳基环丙基酮与非活化烷基溴之间的还原开环反应方法学,进而成功完成一系列烷基酮分子的构建。
Nickel-Catalyzed Regioselective Reductive Ring Opening of Aryl Cyclopropyl Ketones with Alkyl Bromides
B. Yuan, D. Ding, C. Wang, ACS Catal. 2022, 12, 4261. doi: 10.1021/acscatal.2c00677.
正文
目前,通过环丙烷分子参与的开环或扩环反应方法学已经广泛应用于多种有机分子以及关键砌块的构建[1]。这里,受到前期对于环丙基酮开环反应方法学[2]-[7] (Scheme 1A)、Ni(0)催化剂促进的氧化还原中性环丙基酮开环反应方法学[8]-[10](Scheme 1B)以及本课题组长期以来对于还原交叉偶联反应方法学相关研究报道[11]的启发,中国科学技术大学的王川课题组报道一种全新的通过镍催化剂促进的芳基环丙基酮与非活化烷基溴之间的还原开环反应方法学 (Scheme 1C)。
首先,作者采用烷基溴1a与环丙基酮衍生物2a作为模型底物,进行相关还原开环反应条件的优化筛选 (Table 1)。进而确定最佳的反应条件为:采用NiBr2(dme)作为催化剂,L1作为配体,Zn粉作为还原剂,甲醇作为反应溶剂,反应温度为60oC,最终获得88%收率的还原开环产物3aa。
在上述的最佳反应条件下,作者分别对一系列烷基溴底物 (Table 2)以及环丙基酮底物 (Table 3)的应用范围进行深入研究。
接下来,作者通过一系列相关的控制实验研究表明,反应过程中可能并未涉及原位形成的烷基溴化锌试剂(Scheme 2A)。同时,该小组通过相关的化学计量反应研究表明,Zn粉能够同时作为终端还原剂 (terminal reductant),同时能够参与还原步骤中关键中间体的形成 (Schemes 2B-2C)。之后,作者通过氘代实验发现,在反应混合物中存在可烯醇化的相关中间体 (Schemes 2D-2E)。之后,作者进一步发现,反应过程中可能存在通过β-H消除/NiH再插入路径进行的副反应,进而使反应过程中的对映选择性略有降低 (Scheme 2F)。而环丙烷底物中邻近的羰基基团对于反应过程的顺利进行同样较为关键 (Scheme 2G)。接下来,作者进一步观察到,在环丙烷底物的开环反应过程中,两种不同构型的薄荷基溴分子与低价镍催化剂之间的双电子极性氧化加成 (two-electron polar oxidative addition)过程更为有利 (Scheme 2H)。
基于上述的实验研究以及前期相关的文献报道[8]-[10],作者提出如下合理的反应机理 (Scheme 3)。
总结
中国科学技术大学的王川课题组成功设计一种全新的通过镍催化剂促进的芳基环丙基酮与非活化烷基溴之间的还原开环反应方法学,进而成功完成一系列烷基酮分子的构建。这一全新的还原开环策略具有优良的区域选择性、良好的官能团兼容性以及高度的步骤经济性等优势。
参考文献
- [1] (a) J. Liu, R. Liu, Y. Wei, M. Shi, Trends in Chemistry 2019, 1, 779. doi: 10.1016/j.trechm.2019.06.012.
- (b) V. Pirenne, B. Muriel, J. Waser, Chem. Rev. 2021, 121, 227. doi: 10.1021/acs.chemrev.0c00109.
- (c) T. R. McDonald, L. R. Mills, M. S. West, S. A. L. Rousseaux, Chem. Rev. 2021, 121, 3. doi: 10.1021/acs.chemrev.0c00346.
- [2] Y. Yang, M. Shi, Org. Lett. 2006, 8, 1709. doi: 10.1021/ol060415a.
- [3] J. Richmond, V. D. Vuković, J. Moran, Org. Lett. 2018, 20, 574. doi: 10.1021/acs.orglett.7b03688.
- [4] T. Ichiyanagi, S. Kuniyama, M. Shimizu, T. Fujisawa, Chem. Lett. 1997, 26, 1149. doi: 10.1246/cl.1997.1149.
- [5] W. Hao, J. H. Harenberg, X. Wu, S. N. MacMillan, S. Lin, J. Am. Chem. Soc. 2018, 140, 3514. doi: 10.1021/jacs.7b13710.
- [6] S. Agasti, N. A. Beattie, J. J. W. McDouall, D. J. Procter, J. Am. Chem. Soc. 2021, 143, 3655. doi: 10.1021/jacs.1c01356
- [7] Z. Lu, M. Shen, T. P. Yoon, J. Am. Chem. Soc. 2011, 133, 1162. doi: 10.1021/ja107849y
- [8] L. Liu, J. Montgomery, J. Am. Chem. Soc. 2006, 128, 5348. doi: 10.1021/ja0602187.
- [9] S. Ogoshi, M. Nagata, H. Kurosawa, J. Am. Chem. Soc. 2006, 128, 5350. doi:10.1021/ja060220y.
- [10] T.nTamaki, M. Ohashi, S. Ogoshi, Angew. Chem., Int. Ed. 2011, 50, 12067. doi:10.1002/anie.201106174.
- [11] (a) C. Zhang, Z. Lin, Y. Zhu, C. Wang, J. Am. Chem. Soc. 2021, 143, 11602. doi: 10.1021/jacs.1c04531.
- (b) Y. Jin, H. Wen, F. Yang, D. Ding, C. Wang, ACS Catal. 2021, 11, 13355.doi: 10.1021/acscatal.1c04143.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载
本文作者:杉杉
导读
本文主要报道了在无金属催化剂的条件下,以醛为烷基化剂,Et3SiH为还原剂,成功实现了吲哚的还原性N-烷基化反应。同时,该反应具有良好的底物范围,各种取代的芳香族/脂肪族醛和吲哚均为合适的底物。此外,该反应可进行一锅串联1,3-烷基化反应从而合成双烷基化化合物。其中,德克萨斯大学Doug E. Frantz和 百时美施贵宝Albert J. DelMonte为共同通讯作者。
A Metal-Free Reductive N‑Alkylation of Indoles with Aldehydes
Nicholas A. Clanton, Taylor E. Spiller, Eliezer Ortiz, Zhinong Gao, Juan Manuel Rodriguez-Poirier, Albert J. DelMonte,* and Doug E. Frantz*
Org. Lett. 2021, 23, 3233-3236. DOI: 10.1021/acs.orglett.1c00179.
正文
吲哚环骨架广泛存在于各类药物和天然产物中,其中氮取代的吲哚环化合物也备受关注,如美国食品药品监督管理局(FDA)批准的药物中也包含此类骨架(Figure 1)。因此,对于氮取代吲哚环的合成,具有重要的意义。
然而,由于吲哚中氮原子的亲核性较弱,对于吲哚环的N-烷基化反应,具有一定的难度。为了增加亲核性,已使用强碱进行去质子化从而实现活化,但也存在一定的局限性,如与碱敏感性底物不兼容、依赖有毒的烷基化试剂等。此外,也可通过Mitsunobu型方法将醇用作烷基化试剂。同时,醇也被进一步用于“借氢”策略中,通过反应性更高的二氢吲哚中间体实现吲哚的N-烷基化反应。如Seidel等[1] 开发了一种吲哚N-烷基化的方法,涉及衍生自二氢吲哚和醛的瞬态叶立德的氧化还原异构化过程。对于传统的有机金属方法也备注关注,如Hartwig[2]和Trost[3]等报道关于铜催化吲哚和N-甲苯磺酰的偶联反应或π-烯丙基化学反应。最近,通过使用手性过渡金属催化剂也实现了吲哚的不对称N-烷基化反应[4-6]。此外,由于APIs中对于残留金属的量需严格控制,若能通过一种无金属催化的策略,则更具吸引力。受Appleton等[7-9]工作的启发,作者以环己酮为底物,成功在吲哚的C3-位进行烷基化,同时也获得少量的双烷基化副产物3(Scheme 1)。因此,对于C3-烷基化的吲哚底物,可在还原性胺化条件(Et3SiH/TFA),进一步与羰基衍生物进行N-烷基化反应。
首先,作者选择C3-烷基化的吲哚4作为底物,对醛的范围进行了扩展(Table 1)。具有不同取代的芳基醛,均可顺利反应,获得相应的产物6a–6e。同时,一系列脂肪醛也与体系兼容,获得产物6f–6l。值得注意的是,多聚甲醛也可作为甲基化剂,获得产物N-甲基化产物6h。对于6c的克级实验,同样取得预期的结果,收率为86%。
随后,作者选择了几种不同C3-烷基化的吲哚为底物(Table 2),如咔唑均可顺利反应,获得产物8a–8e。同时,吲哚的C3-位上具有羰基官能团时(如酮和酰胺),也与体系兼容,获得产物8g和8h。此外,吲哚的C3-位上为环己基时,可获得产物8f和8i。
此外,作者对反应的实用性进行了相关的研究(Scheme 2)。首先,醛5a可与吲哚4进行N-烷基化反应,合成化合物9,作为亲电试剂用于结构-活性关系(SAR)的研究。其次,醛5b与伯叠氮化物可通过点击化学作为生物连接物,用于生物活性吲哚的细胞靶标鉴定研究,可合成化合物10和11。此外,药物佐米曲普坦(zolmitriptan)也可直接进行N-烷基化反应,获得化合物12。同时,以beclabuvir(1)与环己酮和对甲基苯甲醛为底物,可通过一锅串联C3-烷基/N-烷基化反应,从而以55%的收率得到双烷基化吲哚8i。
随后,作者还对反应的局限性进行了研究(Scheme 3)。当以杂芳基醛为底物(如3-吡啶甲醛和2-糠醛),未能获得N-烷基化产物,可能是由于醛被还原成醇并与N-烷基化反应存在动力学竞争关系。其次,α,β-不饱和醛(如肉桂醛)也不能顺利反应。对于具有空间位阻的醛(如戊醛),也未能进行反应。此外,当吲哚的C3-取代为酰基取代(如15和16)时,由于亲核性降低,导致反应也未进行。对于酮底物(如苯乙酮)也未能和吲哚底物4顺利反应。
总结
本文主要报道了在无金属催化剂的条件下,以醛为烷基化剂,Et3SiH为还原剂,成功实现了吲哚的还原性N-烷基化反应。同时,该反应具有广泛的底物范围、良好的官能团耐受性、温和的反应条件等特点。此外,作者还对反应的局限性也进行了相关的研究。
参考文献
[1] Deb, I.; Das, D.; Seidel, D. Redox Isomerization via Azomethine Ylide Intermediates: N-Alkyl Indoles from Indolines and Aldehydes. Org. Lett. 2011, 13 (4), 812−815. [2] Stanley, L. M.; Hartwig, J. F. Iridium-Catalyzed Regio- and Enantioselective N-Allylation of Indoles. Angew. Chem. Int. Ed. 2009, 48 (42), 7841−7844. [3] Trost, B. M.; Krische, M. J.; Berl, V.; Grenzer, E. M. Chemo-, Regio-, and Enantioselective Pd-Catalyzed Allylic Alkylation of Indolocarbazole Pro-aglycons. Org. Lett. 2002, 4 (12), 2005−2008. [4] Ye, Y.; Kim, S.-T.; Jeong, J.; Baik, M.-H.; Buchwald, S. L. CuH-Catalyzed Enantioselective Alkyation of Indole Derivatives with Ligand-Controlled Regiodivergence. J. Am. Chem. Soc. 2019, 141, 3901−3909. [5] Allen, J. R.; Bahamonde, A.; Furukawa, Y.; Sigman, M. S. Enantioselective N-Alkylation of Indoles via an Intermolecular Aza-Wacker-Type Reaction. J. Am. Chem. Soc. 2019, 141, 8670−8674. [6] Kim, S. W.; Schempp, T. T.; Zbieg, J. R.; Stivala, C. E.; Krische, M. J. Regio- and Enantioselective Iridium-Catalyzed N-Alkylation of Indoles and Related Azoles with Racemic Branched Alkyl-Substituted Allylic Acetates. Angew.Chem. Int. Ed. 2019, 58, 7762−7766. [7] Appleton, J. E.; Dack, K. N.; Green, A. D.; Steele, J. A mild and selective C-3 reductive alkylation of indoles. Tetrahedron Lett. 1993, 34 (9), 1529−1532. [8] Mahadevan, A.; Sard, H.; Gonzalez, M.; Mckew, J. C. A general method for C3 reductive alkylation of indoles. Tetrahedron Lett. 2003, 44 (24), 4589−4591. [9] Rizzo, J. R.; Alt, C. A.; Zhang, T. Y. An expedient synthesis of 3-substituted indoles via reductive alkylation with ketones. Tetrahedron Lett. 2008, 49 (48), 6749−6751.本文作者:杉杉
导读
对于绿色环保亚砜还原策略的开发,一直具有挑战。近日,青岛科技大学郭维斯和文丽荣合作在Green Chemistry上发表论文,报道了一种高效的电化学还原亚砜的策略,可合成一系列硫化物,具有广泛的底物范围、温和的反应条件等特点。此外,Lewis酸AlCl3(通过廉价的铝阳极和氯离子结合从而实现再生)可活化亚砜。
Scalable electrochemical reduction of sulfoxidesto sulfides
Zhenshuo Kong, Chao Pan, Ming Li, Lirong Wen* and WeisiGuo*
Green Chem. 2021, 23, 2773-2777. DOI:10.1039/d1gc00591j
正文
有机硫化物广泛存在于天然产物、药物化学和材料科学中。近年来,已开发出多种硫化物的合成方法。其中,亚砜的还原作为最常用的转化之一,涉及三种经典的反应类型(Scheme 1):(1)催化加氢策略,涉及苛刻的反应条件下以及贵金属的使用。(2)氢化物试剂(如硅烷、硼或硫试剂)的还原策略,但会产生化学计量的副产物。(3)脱氧策略,使用强亲电试剂(三苯基磷和草酰氯)来活化亚砜,但导致官能团耐受性差以及存在一定的副产物。尽管上述方法对于还原亚砜均有效,但大多数均需使用化学计量的还原剂或有毒试剂,从而阻碍了硫化物合成的进一步应用。因此,仍需开发一种通用、可持续的和可扩展的策略来合成一系列硫化物衍生物。
在过去十年中,电化学合成已成为一种高效、绿色环保且可扩展的方法,可用于各种转化。其中,电流可作为氧化还原试剂,从而避免化学氧化剂或还原剂的使用。与阳极氧化相比,对阴极还原的研究较少。在2019年,Baran等[1]使用廉价的镁或铝板作为牺牲阳极,开发了一种电化学Birch还原的策略。最近,Lin等[2]报道了Mg板阳极上烯烃电还原碳官能化反应。此外,Sevov等[3]报道了一种基于Al板阳极的电还原三苯膦氧化物的有效方法。受此启发,作者设想是否可以使用原位生成的Lewis酸来活化亚砜,从而实现亚砜的还原。若可实现,仅需使用廉价得铝板作为牺牲阳极以及亚化学计量的AlCl3。在此,本文将介绍一种电化学还原亚砜的方法,具有底物范围广泛、官能团耐受性高、反应条件温和等特点(Scheme 1)。
首先,作者以1-溴-4-(甲基亚磺酰基)苯1a作为模型底物,进行了相关还原条件的筛选(Table 1)。反应结果表明,当以铝板作为阳极,石墨毡电极作为阴极,DCE作为溶剂,同时加入少量的AlCl3,可在10 mA的恒定电流中室温反应,即可获得94%收率的硫醚产物2a。
在获得上述最佳反应条件后,作者开始对单芳基亚砜底物1进行了扩展(Table 2)。首先,芳基上具有不同给电子和吸电子基团的亚砜,均可顺利反应,获得产物2a–2e。并且,具有酸不稳定Boc保护的亚砜(2c),也可兼容。2-(甲基亚磺酰基)萘底物,以优异的收率获得硫化物2f。对于双(苯亚磺酰基)甲烷底物,还原可得到双(苯硫基)甲烷2g作为唯一产物。对于含有酯基或氨基酸衍生物的亚砜,以中等收率得到产物2h和2i。此外,当使用同时含有亚砜和砜基的底物时,亚砜选择性地还原,获得含砜基的硫化物2j。对于含有环己基、环丙基和吡咯基团的底物,也与体系相容,以高收率生成硫化物2k–2m。对于具有更大空间位阻的亚砜,以46%的收率产生2n。值得注意的是,二烷基亚砜也适合于电化学还原,获得硫化物2o和2p。
随后,作者对二芳基亚砜底物1进行了扩展(Table 3)。当对称的二芳基亚砜的芳基上含有不同的取代基时,均可顺利反应,获得产物3a–3e。同时,具有给电子基的底物收率高于具有吸电子基的底物。其次,含有两个不同芳基的亚砜也被证明是合适的底物,除具有游离羟基(3h,30%)以外,均以极好的收率获得硫化物3f–3j。此外,各种杂环(如吡咯、吡啶、吲哚和噻吩)都可耐受,以高收率获得硫化物3k–3o。对于稠合杂环亚砜底物,也适合于该体系,可获得产物3p–3s。值得注意的是,在还原条件下可耐受羰基基团,如硫化物3q。同时,在优化的条件下,可成功地合成驱虫药阿苯达唑4。
紧接着,作者对反应的实用性进行了研究(Scheme 2)。硫化物2a和3a的克级实验,均具有极好的收率。同时,二苯亚砜的反应可在65 mmol规模上进行,以94%收率获得硫化物3a(11.34 g)。与常规的方法相比,该电还原策略易于扩放大且对环境友好。
随后,作者进行了相关的循环伏安法(CV)实验(Fig. 1)。当使用玻璃碳作为亚砜1a的工作电极,在存在AlCl3时,在-2.4 V处观察到明显的不可逆还原峰,表明生成1a和AlCl3的配合物。
最后,作者提出了一种可能的反应机理(Scheme 3)。首先,AlCl3可与亚砜1配位生成Lewis酸碱配合物A,该配合物通过S-O键断裂,在阴极上进一步还原以获得相应的硫化物2。其次,由牺牲Al阳极产生的Al3+可与氯阴离子结合以再生AlCl3。
总结
青岛科技大学郭维斯和文丽荣合作报道了一种高效且绿色的电化学还原亚砜的策略,可合成一系列硫化物,具有底物范围广泛、反应条件温和等特点。同时,Lewis酸AlCl3(通过廉价的铝阳极和氯离子结合从而实现再生)可活化亚砜。此外,该方法易于放大。
参考文献
[1] B. K. Peters, K. X. Rodriguez, S. H. Reisberg, S. B. Beil, D. P. Hickey, Y. Kawamata, M. Collins, J. Starr, L. Chen, S. Udyavara, K. Klunder, T. J. Gorey, S. L. Anderson, M. Neurock, S. D. Minteer and P. S. Baran, Science, 2019, 363, 838–845. [2] W. Zhang and S. Lin, J. Am. Chem. Soc., 2020, 142, 20661-20670. [3] S. Manabe, C. M. Wong and C. S. Sevov, J. Am. Chem. Soc., 2020, 142, 3024–3031.本文作者 石油醚
概要
Tim J. Donohoe,英国牛津大学化学系教授和牛津大学莫德林学院研究员,有机化学家,课题组主页:http://donohoe.chem.ox.ac.uk/
经历
- 1985-1989年 巴斯大学获得学士学位(Professor T. J. Gallagher)
- 1989-1992年 牛津大学获得博士学位(Prof. S. G. Davies)
- 1993-1994年 博士后研究(Prof. P. D. Magnus FRS)
- 1994-2000年 曼彻斯特大学化学系讲师
- 2000-2001年 曼彻斯特大学化学系读者
- 2001-2004年 牛津大学化学讲师和莫德林学院研究员
- 2004-至今 牛津大学化学系教授和莫德林学院研究员
- 2006-2011年 牛津大学有机化学系主任
获奖经历
- 2015 Editor of Tetrahedron Letters
- 2014 EPSRC Established Career Fellow
- 2014 Royal Society of Chemistry: Charles Rees Award
- 2012 AstraZeneca, GlaxoSmithKline, Pfizer & Syngenta Prize for Process Chemistry Research
- 2011 Royal Society of Chemistry: Synthetic Organic Chemistry Award
- 2006 Royal Society of Chemistry: Corday-Morgan Medal
- 2002 AstraZeneca Award for Organic Chemistry
- 2001 Novartis Young Investigator Award
- 2000 Pfizer Academic Award
- 1998 Glaxo Wellcome award for Innovative Chemistry
- 1998 – 2001 Associate Editor (UK) for the journal Tetrahedron Letters
研究方向
Donohoe小组的研究兴趣在于有机化学对医学和天然产物领域的贡献,以及开发用于有机合成和不对称合成的新方法,利用发展的化学方法来制造具有特殊生物活性的天然产物。
目前在天然产物全合成,转移氢化,氧化,部分还原,钯催化的芳基化等多个方面做出突出的研究。
1. 天然产物全合成1-3
Donohoe小组的研究兴趣在于有机化学对医学和天然产物领域的贡献并开发新方法来对具有生物活性的分子的全合成(Fig.1)。Donohoe小组在有机分子选择性官能化方面的发展了许多新反应,并应用于全合成领域,高效的完成了复杂天然产物的全合成。其中包括:pericosine B, sylvaticin, cis-sylvaticin, hygromycin, dehydromicrosclerodermin B, secosyrin 1, australite, cyclindricine B, lactacystin-β-lactone, deoxypukolide, muscopyridine, streptonigrin and the berberine alkaloids.(Fig.2)
Figure 1 目前的合成目标
Figure 2 已完成的合成目标
2. 转移氢化
目前,Donohoe小组在转移氢化领域变得活跃起来。转移氢化是形成C-C和C-N键的强大催化方法,并且只能将水作为副产物。最初的工作集中于甲醇在烯醇化烷基化中的作用,而最近的研究已经开发了五甲基苯(Ph *)基团,它是借氢位烷基化反应中强大多用途取代基。Donohoe小组应用转移氢化的方法,构建了一系列具有手性的化合物4-11。
Figure 3 转移氢化
3. 氧化反应
Donohoe小组另外一个研究主题是用催化试剂控制烯烃的氧化。Donohoe教授对烯丙基氨基甲酸酯的束缚氨基羟基化的研究以及对机理的做了详细的解释,并将新的一组基于N-O的再氧化剂引入到催化氨基羟基化反应中得到了一种功能更强大,产率更高的氨基羟基化方法。 Donohoe教授将这种方法以特别有效的方式制备氨基环醇(-)-潮霉素的合成。最终通过使用Mitsunobu糖基化反应以仅17个线性步骤(和10%的总收率)完成了天然产物的合成,从而形成了具有良好立体选择性的困难的糖苷键。
Figure 4 氧化反应
对催化由二醇和氨基醇形成四氢呋喃环和吡咯烷环结构的研究表明,利用Os(IV)-(VI)对可以避免Os(VIII)的存在。并发现了OMs置换/氢化物转移序列,然后在分子内捕获氧离子以形成反式THF(由氘标记支持)。在天然产物(+)-顺式-sylvaticin和(+)-sylvaticin的合成中使用了双氧化环化和氢化物转移的组合反应12-16。
Figure 4 氧化反应
4. 选择性还原17-18
Donohoe教授一直在开发使用单电子还原剂(如(催化)LiDBB)部分还原芳香族杂环的兴趣。目前的工作已经能够以选择性和高收率的方式还原吡咯,吡啶和呋喃,通过这种化学方法制备的杂环对于天然(和药用)产品合成具有很大的潜力。课题组部分还原的方法已经在复杂分子的合成中得到了应用。如包括1-epiaustraline, hyacinthcine A1, omuralide and KSM-2690 B. Current targets include cylindricine A and hyacinthacine家族等。
Figure 5 部分还原
其他
1. Chem-station对其题为“[5 + 1]环化催化合成有取代的环己烷”的工作做了介绍。
2. Angew 对Tim J. Donohoe进行了专题介绍。
参考文献
- [1] Donohoe, T. J., Jones, C. R. & Barbosa, L. C. A.Total Synthesis of (±)-Streptonigrin: De Novo Construction of a Pentasubstituted Pyridine using Ring-Closing Metathesis. J. Am. Chem. Soc. (2011) 133, 16418-16421, doi:10.1021/ja207835w.
- [2] Gatland, A. E., Pilgrim, B. S., Procopiou, P. A. & Donohoe, T. J.Short and Efficient Syntheses of Protoberberine Alkaloids using Palladium-Catalyzed Enolate Arylation. Angew. Chem. Int. Ed. (2014) 53, 14555-14558, doi:10.1002/anie.201409164.
- [3] Donohoe, T. J., Jones, C. R., Kornahrens, A. F., Barbosa, L. C. A., Walport, L. J., Tatton, M. R., Baker, D. B.Total Synthesis of the Antitumor Antibiotic (±)-Streptonigrin: First- and Second-Generation Routes for de Novo Pyridine Formation Using Ring-Closing Metathesis. J. Org. Chem. (2013) 78, 12338-12350, doi:10.1021/jo402388f.
- [4] Armstrong, R. J., Akhtar, W. M., Young, T. A., Duarte, F. & Donohoe, T. J.Catalytic Asymmetric Synthesis of Cyclohexanes by Hydrogen Borrowing Annulations. Angew. Chem. Int. Ed. (2019) 58, 12558-12562, doi:10.1002/anie.201907514.
- [5] Smith, L. B., Armstrong, R. J., Matheau-Raven, D. & Donohoe, T. J.Chemo- and Regioselective Synthesis of Acyl-Cyclohexenes by a Tandem Acceptorless Dehydrogenation-[1,5]-Hydride Shift Cascade. J. Am. Chem. Soc. (2020) 142, 2514-2523, doi:10.1021/jacs.9b12296.
- [6] Grozavu, A., Hepburn, H. B., Smith, P. J., Potukuchi, H. K., Lindsay-Scott, P. J. & Donohoe, T. J.The reductive C3 functionalization of pyridinium and quinolinium salts through iridium-catalysed interrupted transfer hydrogenation. Nat. Chem. (2019) 11, 242-247, doi:10.1038/s41557-018-0178-5.
- [7] Akhtar, W. M., Armstrong, R. J., Frost, J. R., Stevenson, N. G. & Donohoe, T. J.Stereoselective Synthesis of Cyclohexanes via an Iridium Catalyzed (5 + 1) Annulation Strategy. J. Am. Chem. Soc. (2018) 140, 11916-11920, doi:10.1021/jacs.8b07776.
- [8] Akhtar, W. M., Cheong, C. B., Frost, J. R., Christensen, K. E., Stevenson, N. G. & Donohoe, T. J.Hydrogen Borrowing Catalysis with Secondary Alcohols: A New Route for the Generation of β-Branched Carbonyl Compounds. J. Am. Chem. Soc. (2017) 139, 2577-2580, doi:10.1021/jacs.6b12840.
- [9] Frost, J. R., Cheong, C. B., Akhtar, W. M., Caputo, D. F. J., Stevenson, N. G. & Donohoe, T. J.Strategic Application and Transformation of ortho-Disubstituted Phenyl and Cyclopropyl Ketones To Expand the Scope of Hydrogen Borrowing Catalysis. J. Am. Chem. Soc. (2015) 137, 15664-15667, doi:10.1021/jacs.5b11196.
- [10] Shen, D., Poole, D. L., Shotton, C. C., Kornahrens, A. F., Healy, M. P. & Donohoe, T. J.Hydrogen-Borrowing and Interrupted-Hydrogen-Borrowing Reactions of Ketones and Methanol Catalyzed by Iridium. Angew. Chem. Int. Ed. (2015) 54, 1642-1645, doi:10.1002/anie.201410391.
- [11] Chan, L. K. M., Poole, D. L., Shen, D., Healy, M. P. & Donohoe, T. J.Rhodium-Catalyzed Ketone Methylation Using Methanol Under Mild Conditions: Formation of α-Branched Products. Angew. Chem. Int. Ed. (2014) 53, 761-765, doi:10.1002/anie.201307950.
- [12] Roushanbakhti, A., Liu, Y., Winship, P. C. M., Tucker, M. J., Akhtar, W. M., Walter, D. S., Donohoe, T. J.Cobalt versus Osmium: Control of Both trans and cis Selectivity in Construction of the EFG Rings of Pectenotoxin 4. Angew. Chem. Int. Ed. (2017) 56, 14883-14887, doi:10.1002/anie.201708278.
- [13] Donohoe, T. J. & Lipiński, R. M.Interplay of Cascade Oxidative Cyclization and Hydride Shifts in the Synthesis of the ABC Spiroketal Ring System of Pectenotoxin-4. Angew. Chem. Int. Ed. (2013) 52, 2491-2494, doi:10.1002/anie.201208919.
- [14] Donohoe, T. J. & Pullin, R. D. C.Natural product synthesis as a challenging test of newly developed methodology. Chem. Commun. (2012) 48, 11924-11938, doi:10.1039/C2CC36040C.
- [15] Donohoe, T. J., Harris, R. M., Williams, O., Hargaden, G. C., Burrows, J. & Parker, J.Concise Syntheses of the Natural Products (+)-Sylvaticin and (+)-cis-Sylvaticin. J. Am. Chem. Soc. (2009) 131, 12854-12861, doi:10.1021/ja9049959.
- [16] Donohoe, T. J., Harris, R. M., Burrows, J. & Parker, J.Total Synthesis of (+)-cis-Sylvaticin: Double Oxidative Cyclization Reactions Catalyzed by Osmium. J. Am. Chem. Soc. (2006) 128, 13704-13705, doi:10.1021/ja0660148.
- [17] Pilgrim, B. S. & Donohoe, T. J.Osmium-Catalyzed Oxidative Cyclization of Dienes and Their Derivatives. J. Org. Chem. (2013) 78, 2149-2167, doi:10.1021/jo302719y.
- [18] Donohoe, T. J., O’Riordan, T. J. C., Peifer, M., Jones, C. R. & Miles, T. J.Asymmetric Synthesis of the Fully Elaborated Pyrrolidinone Core of Oxazolomycin A. Org. Lett. (2012) 14, 5460-5463, doi:10.1021/ol302541j.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!
概要
硫醚或硫代缩醛在雷尼镍的作用下,会发生还原脱硫反应。这是一个把羰基还原成亚甲基的常规方法。
Barton-McCombie反应中使用的自由基还原法(AIBN-Bu3SnH)也能进行同样的脱硫反应。
基本文献
- Pettit, G. R.; van Tamelen, E. E. Org. React.1962, 12, 356.
- radicallic desulfurization: Gutierrez, C. G.; Stingham, R. A.; Nitasaka, T.; Glasscock, K. G. J. Org. Chem. 1980, 45, 3393. DOI: 10.1021/jo01305a004
反应机理
脱硫化后形成的亚甲基上的氢的来源是,在调配雷尼镍时在其金属表面吸附的氢气。
反应实例
典型的反应例子

实验步骤
实验技巧
雷尼镍根据调配的方法不同,其活性差异也很大,另外干燥的时候很容易起火,这个必须非常注意!
为了回避这个缺点,近年来都用、硼化镍Ni2B(= NiCl2+NaBH4)作为替代品,也能达到同样的目的。该试剂不会引起烯烃的还原反应。[1]

参考文献
[1] (a) Brown, C. A. J. Org. Chem. 1970, 35, 1900. DOI: 10.1021/jo00831a039 (b) Brown, C. A.; Ahuja, V. K. J. Org. Chem. 1973, 38, 2226. DOI: 10.1021/jo00952a024[2] (a) Boar, R. B.; Hawkins, D. W.; McGhie, J. F.; Barton, D. H. R. J. Chem. Soc. Perkin Trans. 1973, 654. (b) Zaman, S. S.; Sarmah, P.; Barua, N. C. Chem. Ind.1989, 806 .
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!
- 概要
最常用的还原剂之一。对空气中的水气和氧较稳定,操作处理容易。也能推广适用于工业规模, 因为溶解性的问题,通常使用甲醇、乙醇作为溶剂。
特别是将酮,醛还原到醇的时候,该试剂是首选。反应通常进行的很快,而且简便易行。
通常情况下,硼氢化钠无法还原酯,酰胺,羧酸及腈类化合物,但当酯的羰基α位有杂原子存在时例外,可以将酯还原。(有可能是相邻杂原子的定位作用)。
对于α,β不饱和羰基化合物、优先发生1,4-还原、加入铈盐的话则优先发生1,2-还原(Luche還元)。
- 基本文献
・Schlesinger, H. I. et al. J. Am. Chem. Soc. 1953, 75 , 186. DOI: 10.1021/ja01097a049
・Dalla, V.; Catteau, J. P.; Pale, P. Tetrahedron Lett. 1999, 40, 5193. doi:10.1016/S0040-4039(99)01006-0
- 反应机理
- 反应实例
BF3存在下反应进行时、能将羧酸还原到醇。[1]
碘存在下、体系中可生成BH3-THF络合物,这样一来也可将羧酸还原为醇。[2]
- 实验步骤
- 实验技巧
- 参考文献
[2] McKennon, M. J.; Meyers, A. I.; Drauz, K.; Schwarm, M. J. Org. Chem. 1993, 58, 3568. DOI:10.1021/jo00065a020
概要
羰基化合物被金属氢化物还原生成醇。已知有各种各样的强度性质不同的还原剂。以容易得到,使用方便等实用性来考量,最多被使用的有以下还原剂。
种类
| 硼氢化钠 NaBH4 (Sodium Borohydride) |
| 最常用的一种还原剂,对水分稳定,空气中也能使用,最适合工业生产。溶解性是它的一大问题,通常用甲醇或乙醇作溶剂。酯,酰胺,羧酸不能被还原,但是酯的羰基α位若被杂原子取代的情况下是例外(可能是由于相邻的定位作用)。对于α,β-不饱和羰基化合物,优先发生1,4-还原,加入铈盐的情况下则会优先发生1,2-还原(luche还原)。 |
| 氢化铝锂 LiAlH4 (Lithium Alminium Hydride; LAH) |
| 相当强的还原剂。还原酮,醛不在话下,羧酸和酯也能被还原到对应的醇。腈和酰胺也能被还原,得到胺。卤化物和砜也能被还原,它们原位置上变成氢。它也能使能使环氧化合物发生开环反应。反应一般用到本身不与氢化铝锂发生反应同时有良好的溶解性的THF,乙醚等溶剂。氢化铝锂会与水或质子溶剂发生剧烈反应,放出氢气。由于反应剧烈和容易飞散,不可避免发生火灾。取用时要十分的注意。 |
| 二异丁基氢化铝 (i-Bu)2AlH (Diisobutyl Alminium Hydride; DIBAL) |
| 因为铝原子存在空轨道因此二异丁基氢化铝具有路易斯酸性。因此类似于二异丁基氢化铝这类的ate配位的还原剂常常表现出一些特殊的反应性。腈能被还原到亚胺,然后通过水解最终得到醛。因此腈可以等同看做醛。缩醛能被还原成醚。例如,用DIBAL与亚苄基缩醛反应会得到苄基的醚(参考PMB保护)。另外,在低温条件下进行反应的话,部分情况酯能被还原成醛,这一般不易达到。一般用两个摩尔当量以上的DIBAL先还原到醇之后,再氧化回到醛,要花去很多步骤。而近些年,含有DIBAL的ate型还原剂表现出了这样的部分还原的效果。加入n-BuLi得到的ate型还原剂LiAlH(i-Bu)2(n-Bu),能作为一种非常强的还原剂使用。 |
| 氰基硼氢化钠 NaBH3CN (Sodium Cyanoborohydride) |
| 虽然比硼氢化钠的还原性要弱、但大约在pH3的酸性环境下也能保持稳定是它的一大特点。因此,它经常被用作酸性环境下还原亚胺阳离子。(Borch还原胺化) |
| 硼氢化锂 (Lithium Borohydride) |
| 比硼氢化钠的还原性还要强以至于它能把酯还原到醇。市面有售,也可以通过氯化锂和硼氢化钠制备得到。 |
| 三乙基硼氢化锂 LiBHEt3(Lithium Triethylborohydride: Super-Hydride) |
| 具有非常强的亲核性的氢源,市售的三乙基硼氢化锂都标注着Super-Hydride的字样。被用于卤化物,磺酰基化合物的还原反应。 |
| 硼氢化配体 BH3・L (Borane Complex) |
| 常见的有二甲基硫化硼烷,THF硼烷,均市面有售。比有毒气体的二硼烷要方便使用,作为效果等同于硼烷的还原剂被使用。在酮和羧酸之间选择性还原后者。有双键的情况下会同时发生加成反应,要注意这一点。 |
| 三乙基硅烷 Et3SiH (Triethylsilane) |
| 一般还原反应都是在碱性环境下进行,三乙基硅烷能在TFA等酸性环境下做还原剂使用是它最大的特点。能被用于缩醛的还原,或是糖类的端位烷氧基的消去等。另外,与过渡金属催化剂一起使用可以做硅氢断裂加成。 |
| 二甲氧基乙氧基氢化铝 (Sodium Bis(2-methoxyethoxy)Alminium Hydride; Red-Al) |
| 有和氢化铝锂一样的还原性。不容易起火,适用于大量反应。 |
以下是常用的有选择性的,不单单只是还原反应的试剂。
| 硼氢化镍 Ni(BH4)2 (Nickel Borite) |
| 体系中由NiCl2+NaBH4 得到。氰基和硝基等可以被还原。 |
| 三乙酰基硼氢化钠 NaBH(OAc)3 (Sodium Tri(acetoxy)borohydride) |
一般酸性条件下稳定,和NaBH3CN一样被用于还原胺化反应。另外,β位有未保护的甲氧基的情况,立体选择性还原得到anti-1,3-二醇。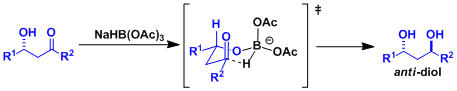 |
| 硼氢化锌 Zn(BH4)2(Zinc Borohydride) |
| 利用锌的螯合能,能发生syn-非对映选择性还原(下図)。常与NaBH(OAc)3 一起使用。
|
| 三异丁基硼氢化锂 LiBH(s-Bu)3 (Lithium Tri(sec-butyl)borohydride; L-Selectride) 三异丁基硼氢化钾 KBH(s-Bu)3 (Potassium Tri(sec-butyl)borohydride; K-Selectride) |
| 强高位阻还原剂、有位阻的部位不发生反应。 |
| Schwartz试剂 Cp2ZrHCl |
| 能与炔或烯发生加成反应,生成的有机锆试剂能进一步用作偶联反应。对硼氢化反应较慢的炔而言可作为有效的催化剂。 |
| Stryker试剂 [(Ph3P)CuH]6 |
| 对于α,β-不饱和羰基化合物,能够优先发生1,4-还原反应。与手性的双齿配体一起使用能催化不对称还原。 |
| 三丁基氢化锡 (n-Bu)3SnH (Tributyl tinhydride) |
| 通常在有自由基引发剂的条件下、用于氢自由基还原。在Pd之类的过渡金属催化剂存在下,经过金属交换发生氢金属化、能得到另一种金属氢化物的中间体。 |
基本文献
反应机理
反应实例
苹果酸乙酯的位置选择性还原[1] 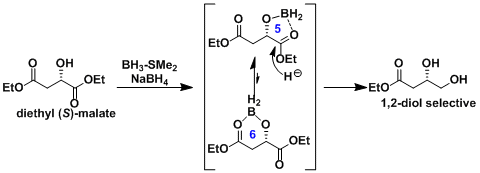 用Me4NHB(OAc)3非对映选择性还原[2]:比NaHB(OAc)3选择性更好。
用Me4NHB(OAc)3非对映选择性还原[2]:比NaHB(OAc)3选择性更好。 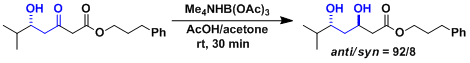 镍的Boc保护胺的第一步变换[3a]:路易斯酸+NaBH4的组合、硝基/叠氮化物/亚胺都可以被还原到胺。[3b-d]
镍的Boc保护胺的第一步变换[3a]:路易斯酸+NaBH4的组合、硝基/叠氮化物/亚胺都可以被还原到胺。[3b-d] 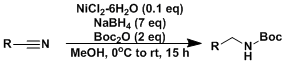
实验步骤
实验技巧
参考文献
[1] Saito, S. et al. Tetrahedron 1992, 48, 4067. doi:10.1016/S0040-4020(01)92187-8[2] Evans, D. A.; Chapman, K. T.; Carreira, E. M. J. Am. Chem. Soc. 1988, 110, 3560. DOI:10.1021/ja00219a035
[3] (a) Caddick, S.; Judd, D. B.; Lewis, A. K. de K.; Reich, M. T.; Williams, M. R. V. Tetrahedron 2003,59, 5417. doi:10.1016/S0040-4020(03)00858-5 (b) Chary, K. P.; Ram, S. R.; Iyengar, D. S. Synlett2000, 683. DOI: 10.1055/s-2000-6614 (c) Cho, B. T.; Kang, S. K. Synlett 2004, 1484. DOI: 10.1055/s-2004-829066 (d) Fringuelli, F.; Pizzo, F.; Vaccaro, L. Synthesis 2000, 646. DOI: 10.1055/s-2000-6389
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!
- 概要
叠氮盐化合物与三价的膦化合物反应、生成亚胺基膦(aza-phosphine ylide)中间体。通过水解得到伯胺的反应叫做Staudinger反应。亚胺基膦是可用作多种化学反应的中间体。也可与羰基反应生成亚胺(aza-Wittig反応)。含有烯烃的伯胺化合物、通过硝基化物Pd催化加氢还原不能制备时,该方法非常有效。
- 基本文献
・Staudinger, H.; Meyer, J. Helv. Chim. Acta 1919, 2, 635. DOI: 10.1002/hlca.19190020164
・Gololobov, Y. G.; Zhmurova, I. N.; Kasukhin, L. F. Tetrahedron 1981, 37, 437.doi:10.1016/S0040-4020(01)92417-2
・Scriven, E. F. V.; Turnbull, K. Chem. Rev. 1988, 88, 297. DOI: 10.1021/cr00084a001
・Gololobov, Y. G.; Kasukhin, L. F. Tetrahedron 1992, 48, 1353. doi:10.1016/S0040-4020(01)92229-X
・Review: Shah, S.;Protasiewicz,J. D. Coord. Chem. Rev. 2000, 210, 181. doi:10.1016/S0010-8545(00)00311-8
・Kohn, M.; Breinbauer, R. Angew. Chem. Int. Ed. 2004, 43, 3106. DOI: 10.1002/anie.200401744
- 反应机理
参考:J. Org. Chem. 2004, 69 , 4299. J. Am. Chem. Soc. 2005, 127, 2686.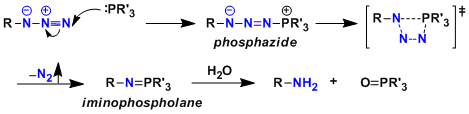
- 反应实例
Staudinger-Bertozzi配合[1]:Bertozzi等将叠氮化物与以下的膦试剂反应,成功将荧光试剂与强固的酰胺连接。这一化学修饰法以高収率、高化学选择性进行、能用于多种生物化学研究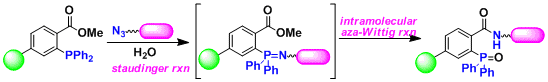
Traceless Staudinger Ligation[2]:需要Cys残基组Native Chemical Ligation没有特别的制约。
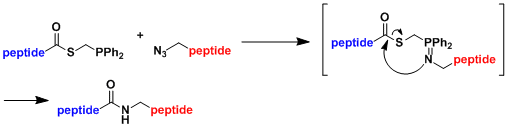
- 实验步骤
- 实验技巧
- 参考文献
[2] (a) Saxon, E.; Armstrong, C.R.; Bertozzi, C.R. Org. Lett. 2000, 2, 2141. DOI: 10.1021/ol006054v (b) Nilsson, B.L.; Kiessling, L.L.; Raines, R.T. Org. Lett. 2000, 2, 1939. DOI: 10.1021/ol0060174